Полные и сокращенные ионные уравнения для Cu(OH)2 и HCl
На этой странице вы найдете подробную информацию о реакциях между гидроксидом меди(II) и соляной кислотой. Мы предоставим как полные, так и сокращенные ионные уравнения, а также полезные советы по их составлению и пониманию.
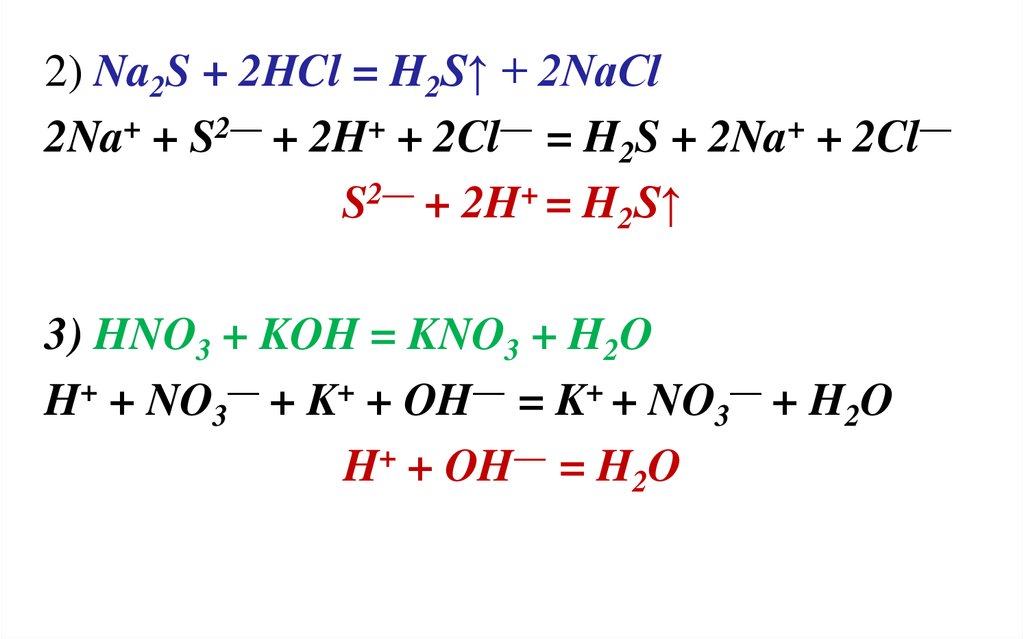

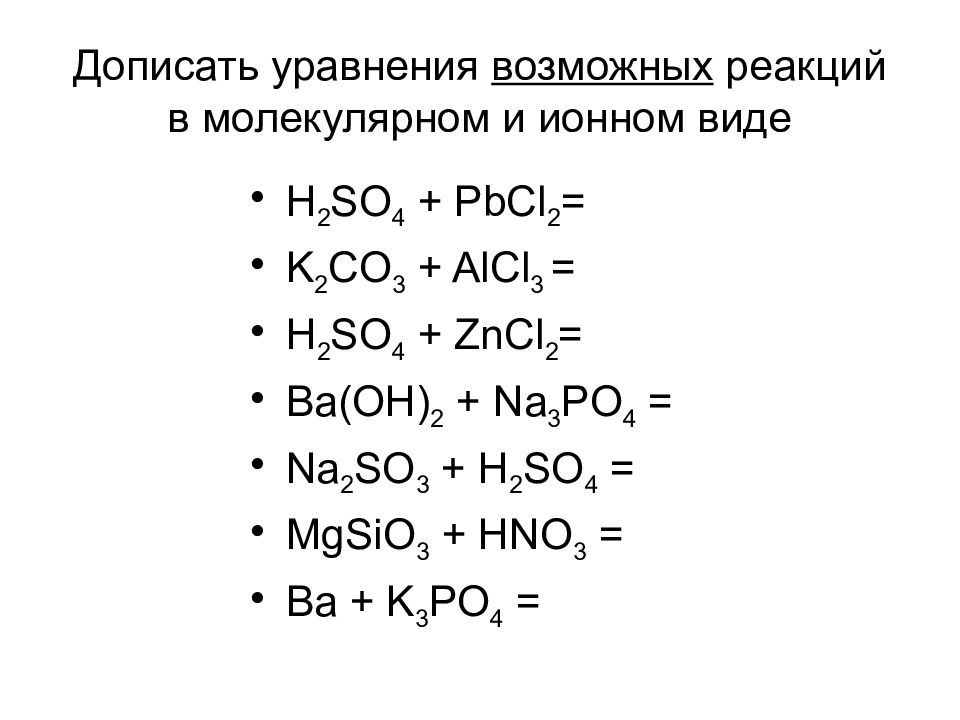
При составлении полного ионного уравнения всегда начинайте с написания молекулярного уравнения реакции.
РЕАКЦИИ ИОННОГО ОБМЕНА и условия их протекания - Как составлять молекулярные и ионные уравнения


Для правильного написания ионного уравнения важно понимать, какие вещества диссоциируют в растворе.
Decomposition of Cu(OH)2
Не забывайте проверять равенство числа атомов каждого элемента и заряда в обоих частях уравнения.

Cu(OH)2 в растворе практически не растворяется, поэтому его записывают как твердое вещество (осадок) в уравнении.
РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по Химии

HCl в водном растворе полностью диссоциирует на ионы H+ и Cl-, что необходимо учитывать при составлении ионного уравнения.
Разложение гидроксида меди II (Cu(OH)2 = CuO + H2O)
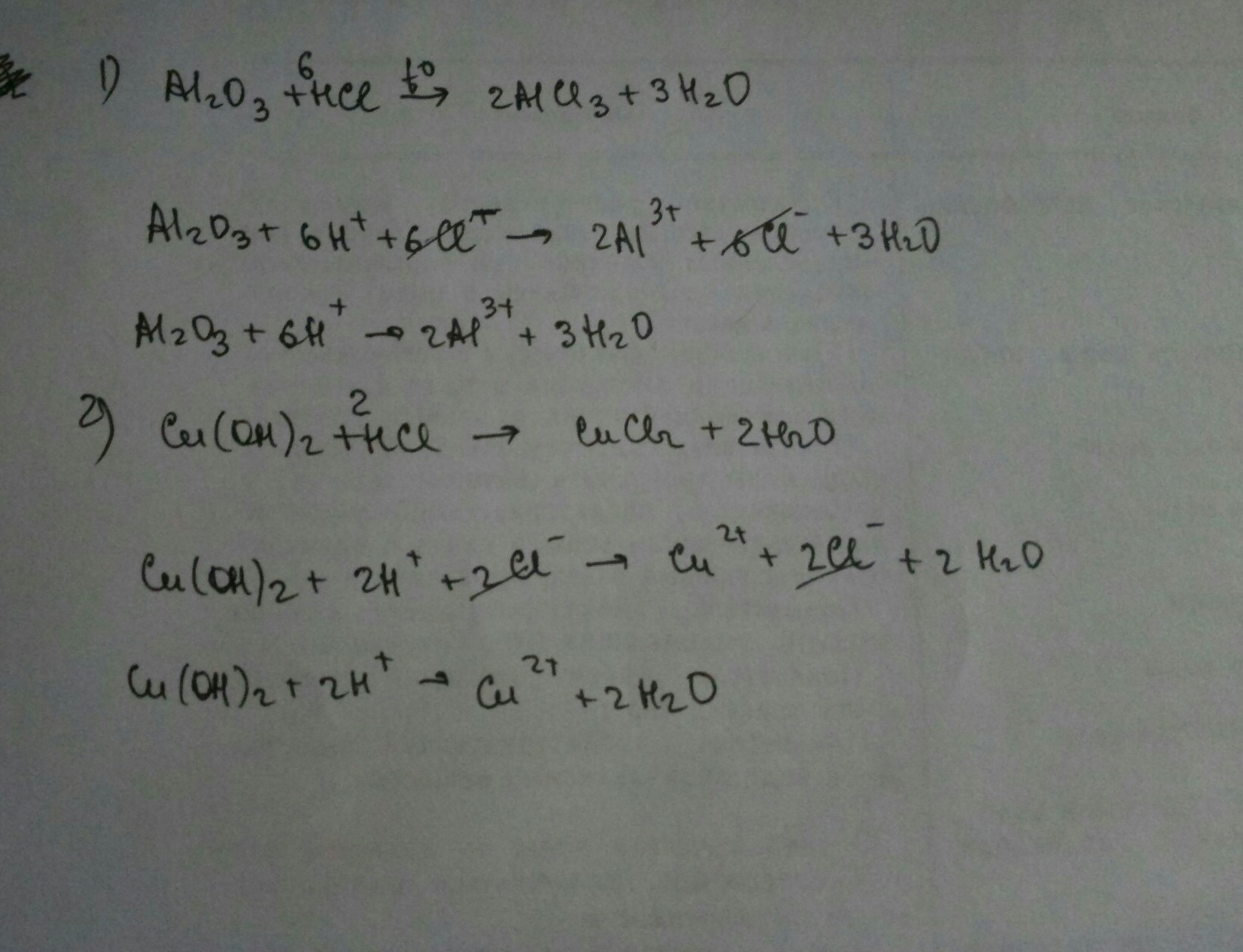

При написании сокращенного ионного уравнения уберите ионы, которые не участвуют в химической реакции (зрительские ионы).
Для проверки правильности уравнения можно использовать метод электронного баланса.
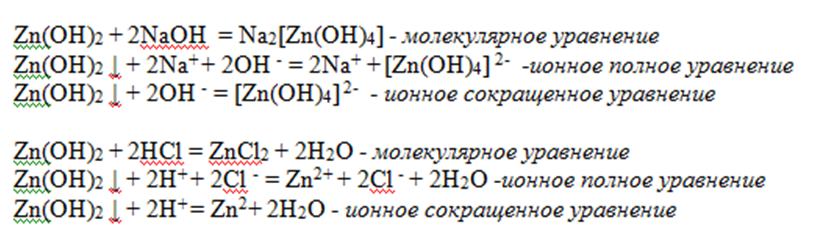
Изучение ионных уравнений помогает лучше понять процессы, происходящие в растворах.

Практикуйтесь в написании различных ионных уравнений, чтобы закрепить свои навыки и уверенность в теме.

Используйте таблицы растворимости и диссоциации, чтобы избежать ошибок при составлении уравнений.