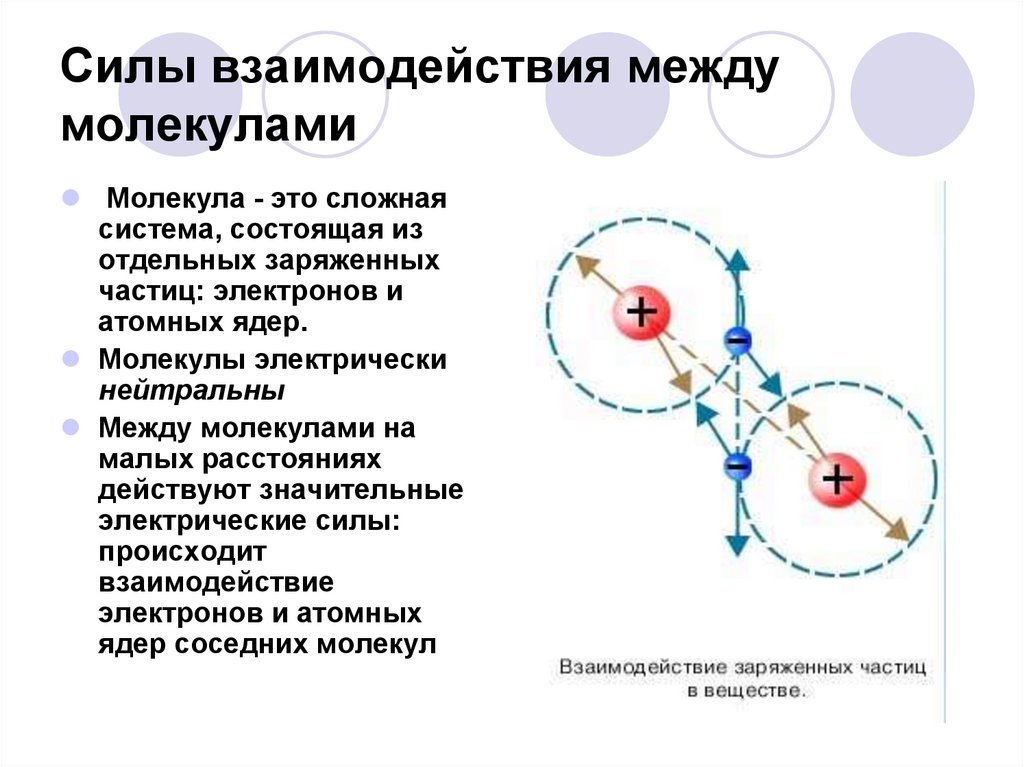
Основы сил взаимодействия между молекулами в физике
В этом разделе представлены фотографии и полезные советы по теме взаимодействия между молекулами, раскрывающие физические аспекты этих процессов и объясняющие механизмы их действия.
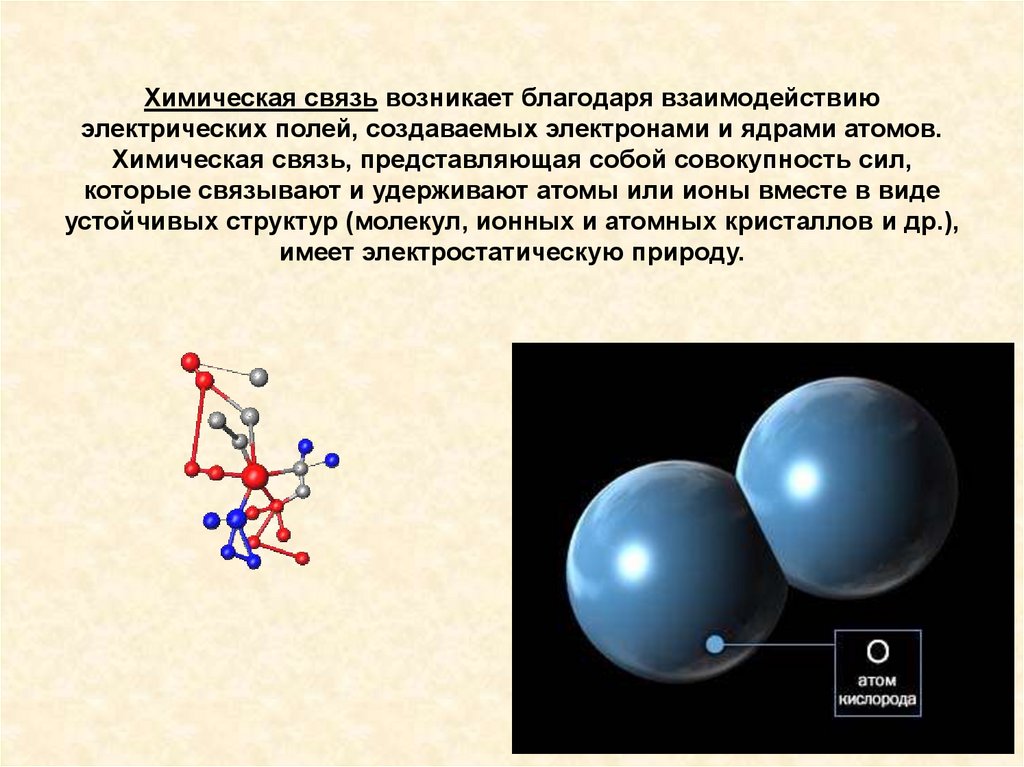

Изучите типы межмолекулярных сил: ван-дер-ваальсовы, диполь-дипольные и водородные связи.
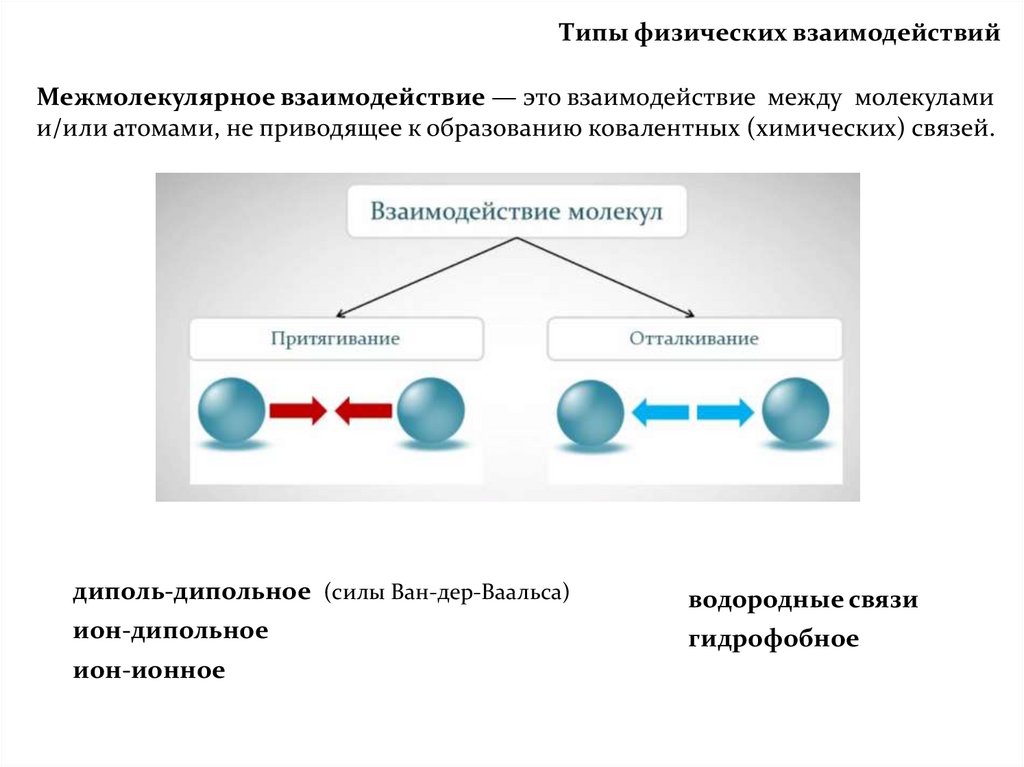
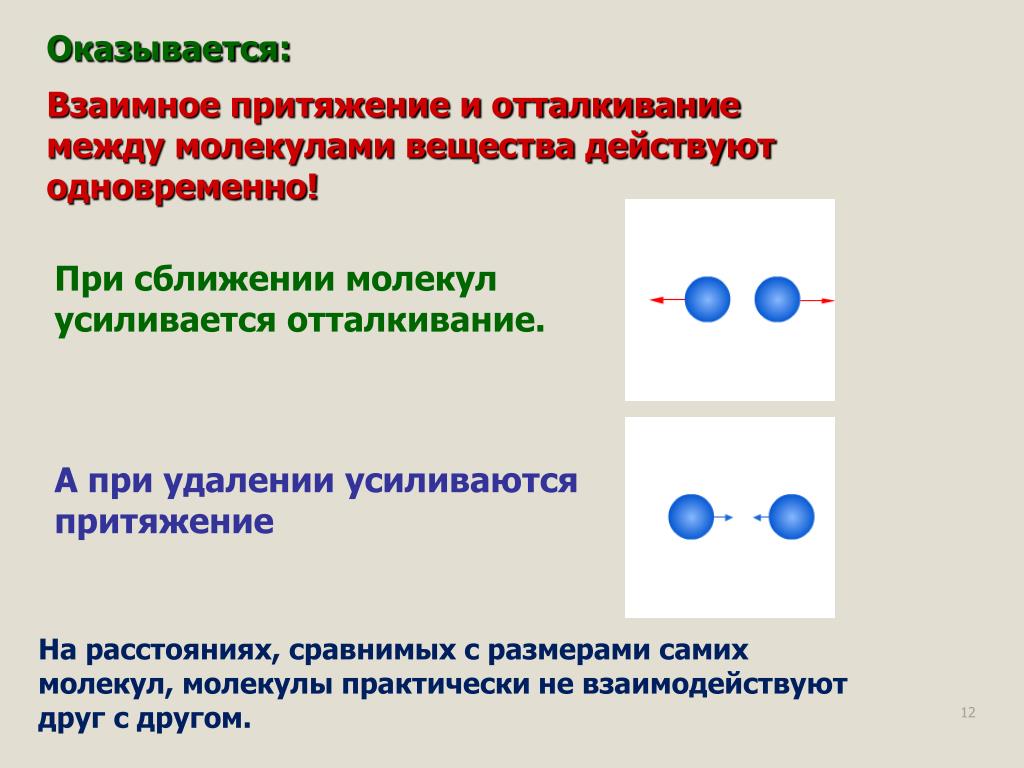
Помните, что сила взаимодействия зависит от расстояния между молекулами: чем ближе молекулы, тем сильнее взаимодействие.
Водородная связь особенно важна в биологических системах, таких как ДНК и белки.
Действие сил притяжения и отталкивания между молекул
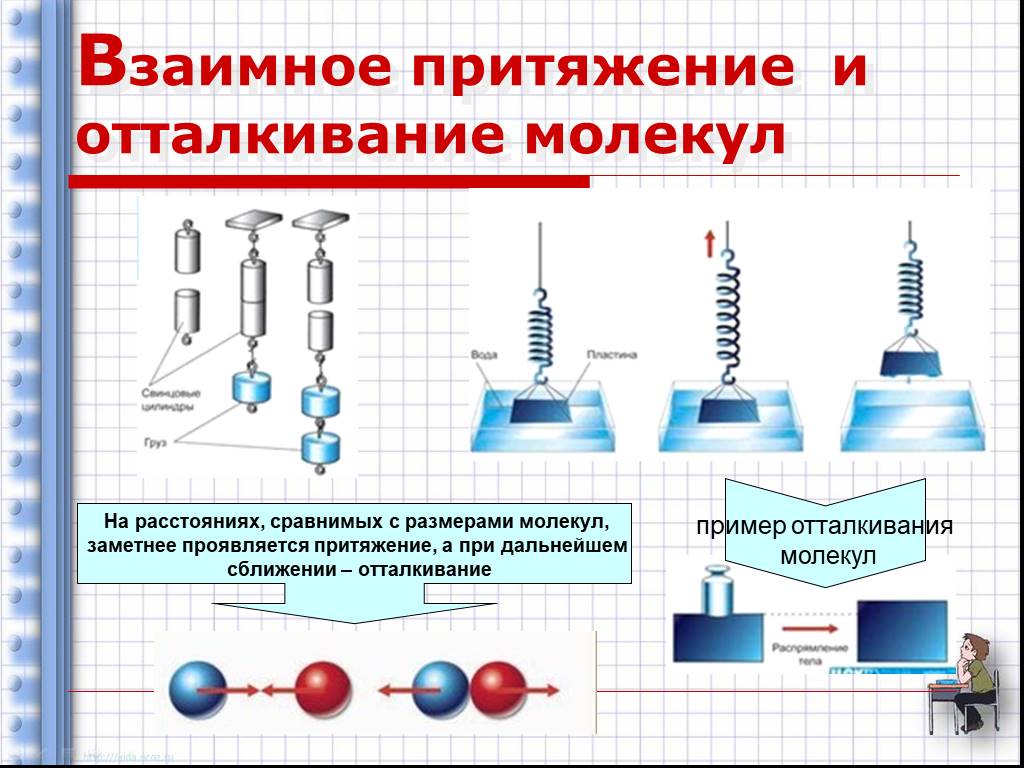
Межмолекулярные силы играют ключевую роль в определении физических свойств веществ, таких как температура плавления и кипения.
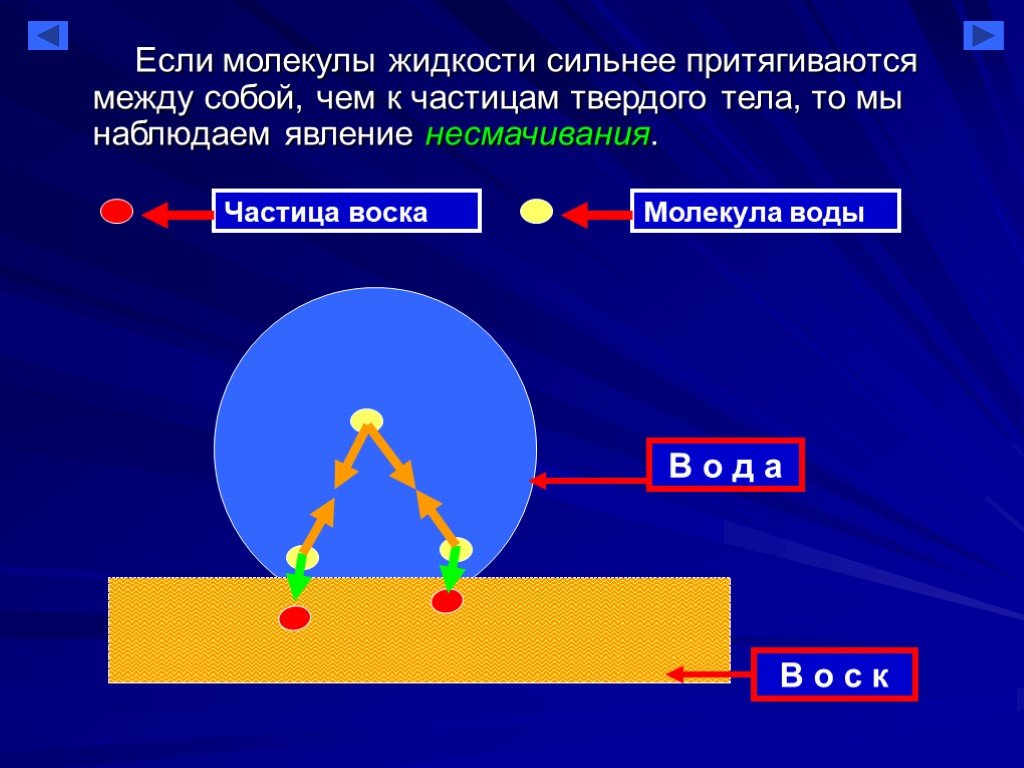
Ван-дер-ваальсовы силы проявляются во всех молекулах, но особенно важны для неполярных веществ.
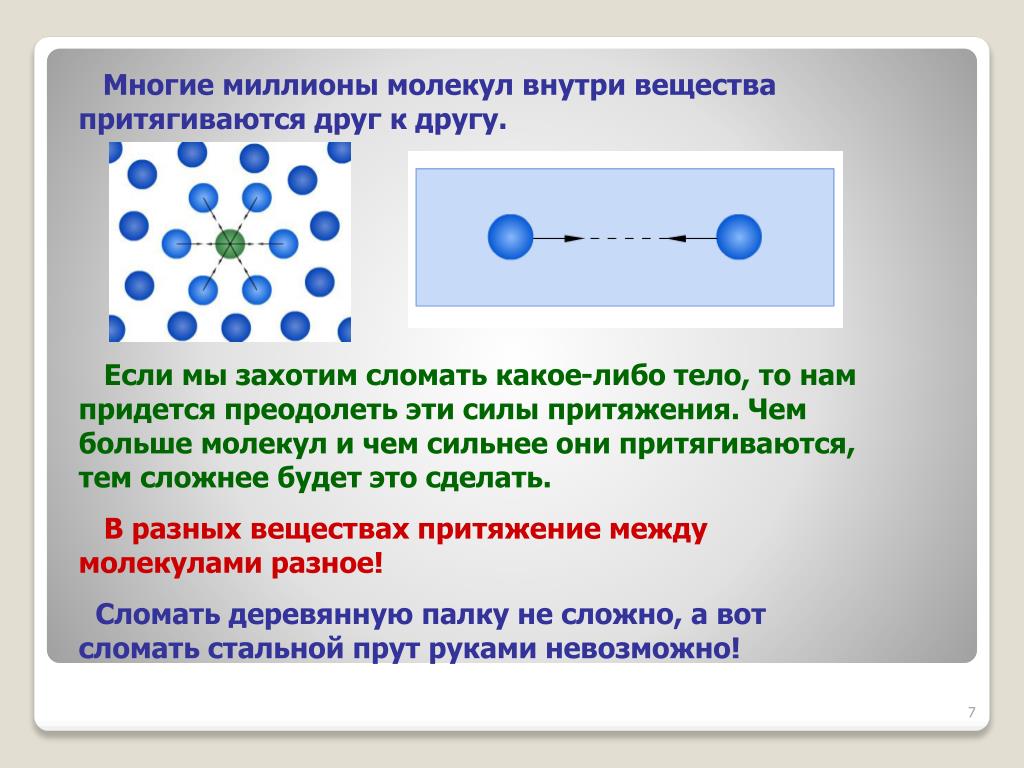
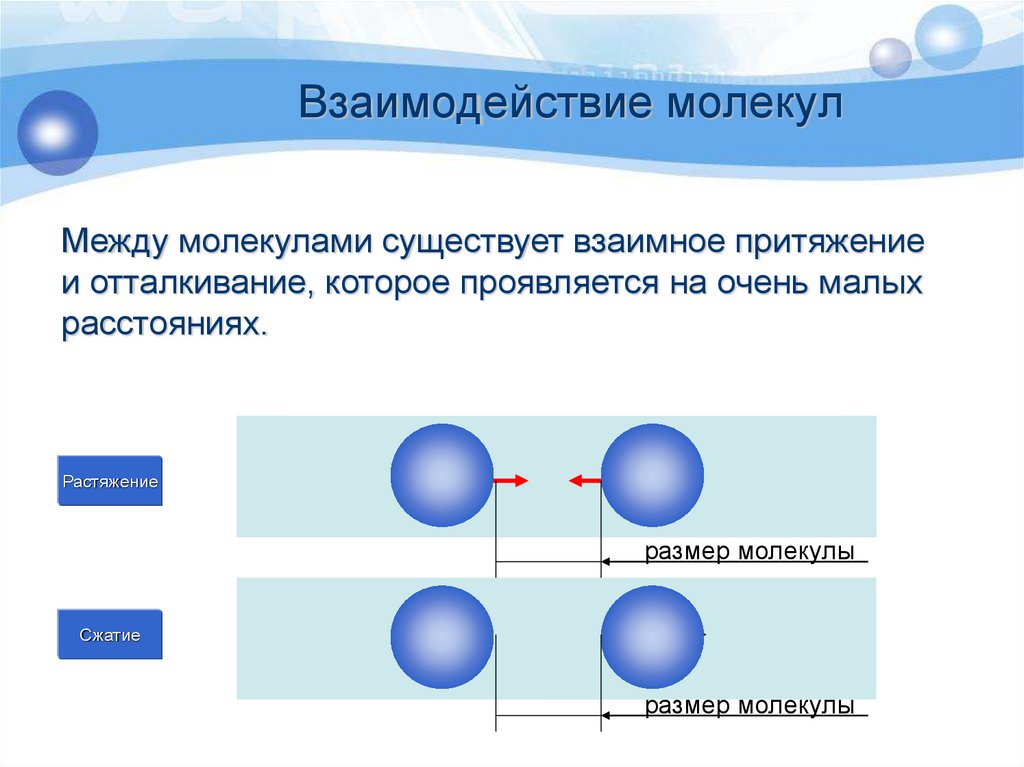
Используйте модели и визуализации для лучшего понимания пространственного расположения молекул и их взаимодействий.
Запомните, что межмолекулярные силы значительно слабее, чем ковалентные и ионные связи внутри молекул.

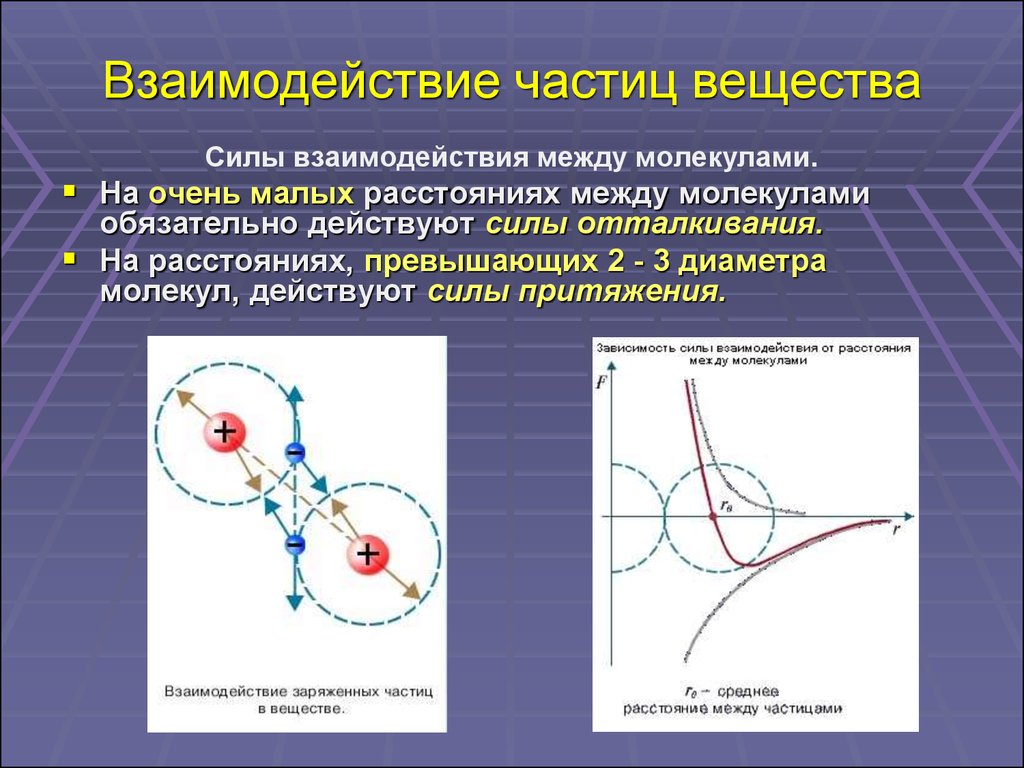
Диполь-дипольные взаимодействия важны для полярных молекул, таких как вода.

При изучении межмолекулярных сил обратите внимание на влияние внешних условий, таких как температура и давление.
Межмолекулярные взаимодействия: скрытые силы, управляющие веществом

Понимание межмолекулярных взаимодействий помогает объяснить многие физические и химические свойства материалов.